付 胃悪性リンパ腫診療の手引き
- はじめに
- A 胃悪性リンパ腫の診断
- B 胃 MALT リンパ腫
の治療 - C びまん性大細胞 B 細胞性リンパ腫(DLBCL)の治療
びまん性大細胞B細胞性リンパ腫(DLBCL)の治療
化学療法,放射線治療
初発
1)進行期(Lugano 分類30)でⅡ2 期以上)
DLBCL は進行期であっても治癒が望める悪性腫瘍であり,全身性の DLBCL と考え,手術や放射線治療のような局所療法単独治療は行わない。現在では,成人の全年齢層において抗 CD20 モノクローナル抗体(リツキシマブ)併用 CHOP(シクロホスファミド,ドキソルビシン,ビンクリスチン,プレドニゾロン)療法(R-CHOP 療法),6~8コースが基本的な標準治療である31-36)。国際予後指標(InternationalPrognostic Index;IPI)での予後不良因子(61歳以上,病期Ⅲ以上,PS2 以上,血清 LDH 高値,節外病変 2個以上)が 3個以上ある場合は予後不良37)であり,RCHOP 療法6~8コースを実施するか,臨床試験として自家造血幹細胞移植併用の大量化学療法(HD-SCT)や新規薬剤による治療などが実施される31-33)。
2)限局期(Lugano 分類30)で病期Ⅱ1 期まで)
手術後化学療法3~4コースの治療群と化学療法単独群の治療成績は変わらないという報告38)もあるが,ドイツ39)や日本40)から報告されたように手術した場合と化学療法放射線併用し,胃を温存した場合の全生存は変わらないため,現在では手術の適応は穿孔や止血困難な出血がある場合などに限られている31,41)。化学療法による組織の壊死で穿孔や出血が生じる可能性があるため手術が治療法の選択にあげられるが,壊死や穿孔のリスクの高い症例を明確に示唆するものは報告されていない。
胃原発を含む限局期 DLBCL は,巨大腫瘤病変や予後不良因子(61歳以上,病期 Ⅱ期,血清 LDH 高値,PS2 以上)を認めない限局期において CHOP 療法3コース後放射線治療群と CHOP 療法8コース群を比較した結果,CHOP 療法後放射線治療群は5年の無増悪生存率が77%,全生存率が82%と CHOP 療法単独群より有意に優れていたため CHOP 療法3コース後放射線治療群が予後不良因子のない標準治療となった42)。しかし,① 長期間のフォローアップをすると CHOP 療法 3コース+放射線治療群で晩期再発が多い傾向がみられる,② CHOP 療法8コース終了後放射線治療(30Gy)の有無で比較した臨床試験で,放射線治療追加群は無病生存期間の延長や局所コントロールは可能になるが全生存期間は変わらない43),60歳以上のリスク因子のない患者では CHOP 療法 4コースと CHOP 療法 4コース実施後放射線治療(40Gy)群との無作為比較試験の結果で全生存期間は変わらない44)などの報告があり,放射線治療の位置づけはやや不明瞭とも考えられる。ただし,対象患者が少し異なることや長期間のフォローが完全でないことなどから現時点で放射線治療が不要と結論づけることはできない。
限局期胃 DLBCL のような予後良好群に R-CHOP 療法を行うことで,さらに治療成績を改善させられるかが議論されてきたが,(1)前述したように進行期DLBCLの標準治療は R-CHOP 療法であることと,(2)主に限局期 DLBCL を対象とした臨床試験(MInT study)において IPI=0 の低リスク群においてもリツキシマブ併用化学療法が化学療法単独に比べてすぐれた結果を示していること36),(3)historical control との比較で,preliminary なデータであるが,限局期 DLBCL 全体では R-CHOP 療法+放射線治療の成績が CHOP 療法+放射線治療より良好なため45),実際は RCHOP 療法+放射線治療が行われることが多い。そのため,現在の治療方針として NCCN のガイドラインでは,① 前述の予後不良因子がない場合は R-CHOP 療法3コース後放射線治療,② 予後不良因子がある場合は R-CHOP 療法 6~8コースもしくは R-CHOP 療法3コース後放射線治療が推奨されるとなっているが,PET を用いた治療効果判定基準が提唱されており46),今後化学療法後放射線治療の対象となる患者は減少するかもしれない。また,胃腫瘤の大きさと治療方法の選択にコンセンサスのある明確な基準はないが,参考として NCCN ガイドライン31)では10cm以上の巨大腫瘤病変がある場合は R-CHOP 療法6~8コース後放射線治療が推奨されるとなっている。

再発時
救援化学療法が奏効する場合は,治癒がまだ望めるため高齢者を除いては自家造血幹細胞移植併用の大量化学療法が推奨されている47)。
救援化学療法として ESHAP(エトポシド,メチルプレドニゾロン,シタラビン,シスプラチン)療法,DeVIC 療法(デキサメタゾン,エトポシド,イフォスマイド,カルボプラチン),EPOCH(エトポシド,プレドニゾン,ビンクリスチン,シクロホスファミド,ドキソルビシン)療法などが実施されることが多い31,32)。
外科治療
StageⅠ-Ⅱ1 の DLBCL については,胃癌に準じた D2 郭清を伴う胃切除術を行うことにより,手術単独による治療でも90%程度の5年生存率を得ることができるとの報告がある48)。しかし,再発は5年を過ぎてもみられている。外科的切除後の再発の特徴は遠隔のリンパ組織に再発している点である。DLBCL は一般に放射線治療と化学療法の組み合わせで治療されているが,手術は局所療法であり,強いていえば放射線治療に置き換わるものである。したがって,何らかの理由で照射を避け,外科治療を行った場合には,化学療法を追加しない限り,標準療法と同等とはいえない。反面,化学療法を行わない場合でも,胃癌に準じた手術を行うことにより,治癒の可能性は残される。
手術療法の適応は限られるが,非外科的治療中に起きた大量出血や穿孔などの合併症への対処と,稀な不応例に対する salvage としての外科治療は今後も行われることになる。合併症が起きた場合には骨髄抑制の最中に緊急手術を行うことになり,手術のリスクは高い。しかし,その後も同様の治療を継続することを考えると,合併症のもととなった胃病変を残すことは賢明とはいえないので,可能な限り主病巣の切除を行うことになる。系統的なリンパ節郭清にこだわらず,必要最低限の手術にとどめるのが現実的であると思われる。一方,治療不応例に対しては,外科治療で根治を求める立場から,胃癌に準じたリンパ節郭清を伴う根治的な手術を行うことになる。占居部位や腫瘍の大きさゆえに胃全摘が必要となる可能性が高い。
なお,わが国における非外科的治療を検証する第2相試験では,StageⅠ-Ⅱ1症例52例が集積され,48 例で CR が得られ,salvage surgery は不応例2例に行われたのみであった。穿孔や大量出血は認められず,94%の2年生存率が報告されている49)。
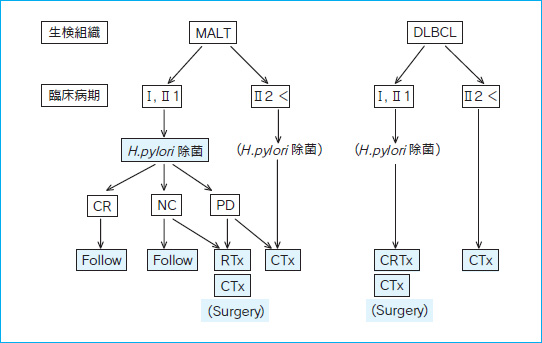
図 1 胃 MALT リンパ腫および胃 DLBCL の治療の流れ
MALT:MALT リンパ腫,DLBCL:びまん性大細胞 B 細胞性リンパ腫
臨床病期:Lugano 国際会議分類(表 1 参照)
CR:Complete response,NC:No change,PD:Progressive diseas
RTx:Radiation therapy,CTx:Chemotherapy,CRTx:Chemoradiation therapy
MALT リンパ腫の H. pylori 除菌への NC 例に対する二次治療の追加時期や方法に関しては,いまだ統一された見解はない。