Ⅱ章 治療法
内視鏡的切除
内視鏡的切除の種類(CQ11)
EMR(Endoscopic Mucosal Resection)
胃の粘膜病変を挙上して鋼線のスネアをかけ,高周波により焼灼切除する方法である14,15)。
ESD(Endoscopic Submucosal Dissection)
高周波デバイスを用いて病巣周囲の粘膜を切開し,さらに粘膜下層を剝離して切除する方法である16‒18)。
内視鏡的切除における標本の取扱い
標本の取扱い
切除標本の取扱いは,『胃癌取扱い規約第15版』に準ずる。
分化型癌と未分化型癌
生検および内視鏡的切除後の組織像について,分化型癌と未分化型癌を区別する。『胃癌取扱い規約第15版』の組織型分類のうち,悪性上皮性腫瘍・一般型のpap,tub1,tub2を分化型癌とし,por1,por2,sigを未分化型癌とする。なお,SM浸潤部でmucを有する例については,分化型癌・未分化型癌どちらの由来であるかにかかわらず,現時点では未分化型に準じて取扱う。
組織学的優位性およびULの評価
分化型癌と未分化型癌が混在する場合は,優勢な組織像に従って分類する。また複数の組織型が混在する場合は,量的に優勢な組織型から順に記載する(tub2>tub1など)。ULは組織学的なULの存在をもってUL1と判定するが,ULの判定はしばしば病理学的にも困難なことがあり,術前の生検瘢痕が潰瘍瘢痕とされることがある。したがって,内視鏡やX線等の画像診断所見,さらに術前生検の有無を臨床的に考慮して,治療の方針は担当医が最終判断することが望ましい。一般的に,生検瘢痕は粘膜筋板直下の小範囲に限局した線維化としてとらえることができる19)。しかし生検瘢痕と潰瘍瘢痕の区別ができないときはUL1と判定する。
内視鏡的切除の適応
本ガイドラインでは,リンパ節転移の危険性が1%未満と推定される病変を,外科的胃切除と同等の成績が得られると考え,「絶対適応病変」として定義した。また,リンパ節転移の危険性は1%未満と推定されるものの,長期予後に関するエビデンスに乏しい病変を「適応拡大病変」とした。さらに,外科的胃切除が標準治療となる病変の中にも,内視鏡的切除により治癒する可能性があるものがあり,外科手術を選択し難い状況があることを鑑み,こうした病変を「相対適応病変」とした。
適応の原則
リンパ節転移の可能性が極めて低く20),腫瘍が一括切除できる大きさと部位にあること。
適応
1)絶対適応病変21,22)
①EMR/ESD適応病変
・2 cm以下の肉眼的粘膜内癌(cT1a),分化型癌,UL0,と判断される病変。
②ESD適応病変
・2 cmを超える肉眼的粘膜内癌(cT1a),分化型癌,UL0,と判断される病変。
・3 cm以下の肉眼的粘膜内癌(cT1a),分化型癌,UL1,と判断される病変。
2)適応拡大病変23)
・2 cm以下の肉眼的粘膜内癌(cT1a),未分化型癌,UL0,と判断される病変。この条件を満たす病変は,現時点では長期予後に関するエビデンスが乏しいため,JCOG1009/1010試験等の結果が出るまでは,絶対適応としない。
3)相対適応病変
上記1),2)以外の病変の標準治療は外科的胃切除である。しかし,年齢や併存症など何らかの理由で外科的胃切除を選択し難い早期胃癌の場合には,推定されるリンパ節転移率などを考慮しつつ,内視鏡的切除が選択される場合があり得る。その場合は相対適応として,標準治療は外科的胃切除であること,リンパ節転移の危険性などの説明を十分に行い,患者の理解と同意が得られた場合のみ施行する。
遺残再発病変に対する適応24)
初回のEMR/ESD時の病変が絶対適応病変で,その後に粘膜内癌で局所再発した病変であれば,適応拡大病変として取扱うことが可能である。しかし,再ESDを支持する明確なエビデンスはなく,症例数の多い長期経過観察のデータの集積が望まれる。
内視鏡的切除の根治性
根治性の評価
EMRおよびESDの根治性は,局所の切除度とリンパ節転移の可能性という2つの要素によって決定される。
1)内視鏡的根治度A(eCuraA)
腫瘍が一括切除され,
①UL0の場合,腫瘍径を問わず,分化型癌優位で,pT1a,HM0,VM0,Ly0,V0,
②UL1の場合,3 cm以下の分化型癌優位で,pT1a,HM0,VM0,Ly0,V0
であること。
これらが満たされた場合を内視鏡的根治度A(eCuraA)とする。ただし,①で,未分化型成分が長径で2 cmを超えるものは内視鏡的根治度C‒2とする。
2)内視鏡的根治度B(eCuraB)
腫瘍が一括切除され,切除標本が,①2 cm以下のUL0,未分化型癌優位でpT1a,②3 cm以下の分化型癌優位でpT1b(SM1)(粘膜筋板から500μm未満),のいずれかであり,かつHM0,VM0,Ly0,V0であった場合を内視鏡的根治度B(eCuraB)とする。
ただし,②でSM浸潤部に未分化型成分があるものは内視鏡的根治度C‒2とする25)。
3)内視鏡的根治度C(eCuraC)
上記の内視鏡的根治度A,Bに当てはまらない場合を内視鏡的根治度C(eCuraC)とする。
①内視鏡的根治度C‒1(eCuraC‒1)
分化型癌の一括切除で側方断端または分割切除のみが内視鏡的根治度A,Bの基準から外れる場合。
②内視鏡的根治度C‒2(eCuraC‒2)
上記,内視鏡的根治度A,B,C‒1のいずれにも当てはまらない場合。
内視鏡的切除後の治療方針
切除後の病理診断により根治度の判定を行い,その後の方針を決定する。
内視鏡的根治度A(eCuraA)の場合
年に1~2回の内視鏡検査による経過観察が望ましい26)。
内視鏡的根治度B(eCuraB)の場合
経過観察では,年に1~2回の内視鏡検査に加えて,腹部超音波検査,CT検査などで転移の有無を調べることが望ましい27,28)。
a,bいずれの場合もヘリコバクター・ピロリ感染の有無を検査し,陽性者では除菌を行うことが推奨されている(CQ12)。しかし,除菌の有無による異時性多発胃癌発生に差がないという報告もあり,さらなる検討が必要である29,30)。
内視鏡的根治度C(eCuraC)の場合
①内視鏡的根治度C‒1(eCuraC‒1)
転移の危険性は低く,この場合には,施設の方針により,患者への十分な説明と同意を得た後,再ESD,追加外科切除,切除時の焼灼効果(burn effect)に期待した慎重な経過観察,焼灼法(レーザー,アルゴンプラズマ凝固など)を選択する31)。ただし,①分化型,pT1a(M),UL1,3 cm以下,および②分化型,pT1b(SM1),3 cm以下,の場合には内視鏡を再検し遺残の大きさを確認し,遺残癌の大きさとESD標本内の癌の大きさの合計が30 mmを超える場合は原則追加外科切除とする。また,SM浸潤部で分割切除あるいは断端陽性になった場合にも,病理診断そのものが不確実となるため,追加外科切除とする。
②内視鏡的根治度C‒2(eCuraC‒2)
原則として追加外科切除が標準である。年齢や合併症など何らかの理由で外科的胃切除を選択しない場合には,表2,表3に示したようなリンパ節転移の危険性や,局所再発,遠隔転移などのデータから根治性を評価し,十分に説明する必要がある。また再発した場合には根治が困難であり,予後不良であることを説明し,最終的に患者の十分な理解と同意を得なければならない。
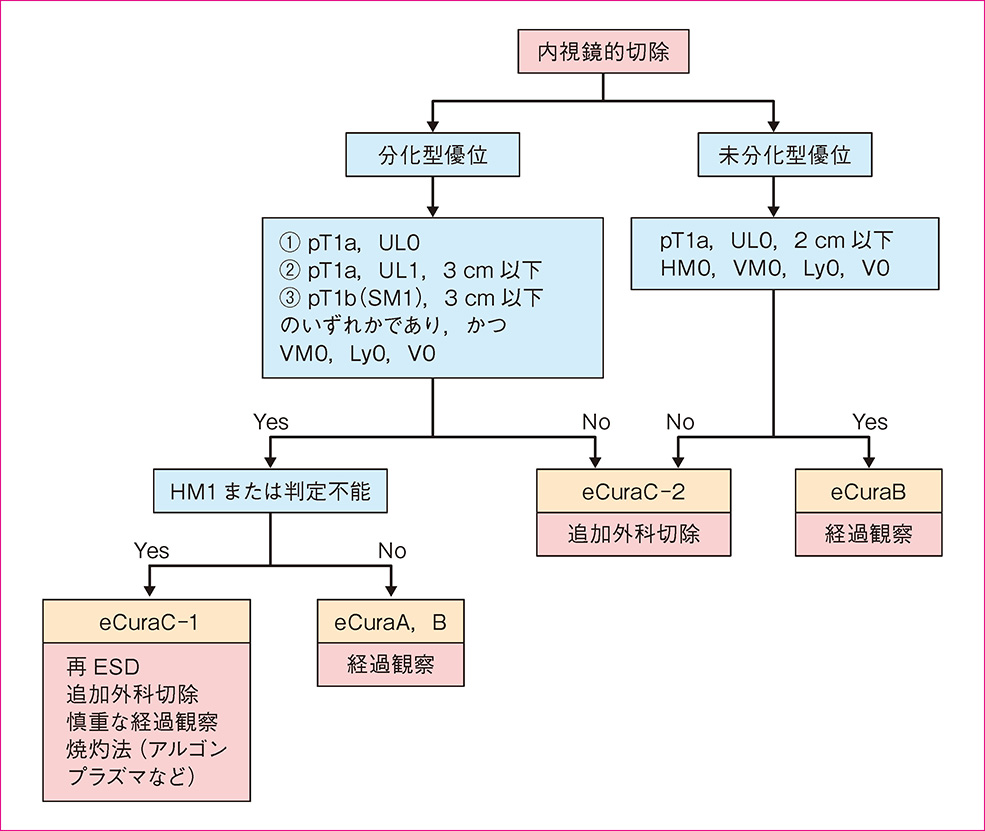
図 7 内視鏡的切除後の治療方針アルゴリズム
表 2 外科切除例からみた早期胃癌のリンパ節転移頻度32)
(国立がん研究センター中央病院,がん研有明病院)
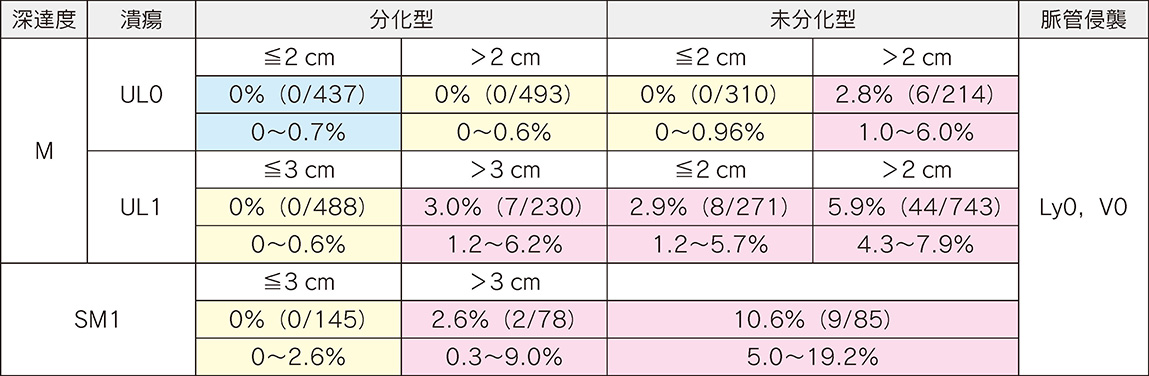
上段:リンパ節転移率,下段:95%信頼区間
表 3 ESD後追加外科切除例からみたリンパ節転移頻度33)
(腫瘍径3 cm超,深部断端陽性,静脈侵襲あり,SM2以深の場合にそれぞれ1点,リンパ管侵襲ありの場合に3点を付与した合計点による)
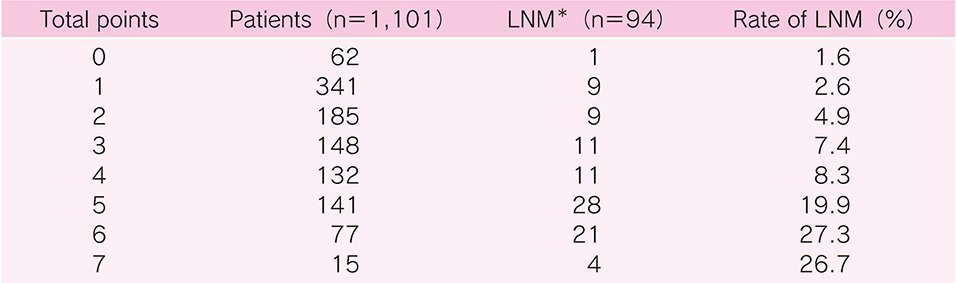
*LNM:lymph node metastasis